COVID-19
Coronavac é suspensa no RN por recomendação da Anvisa
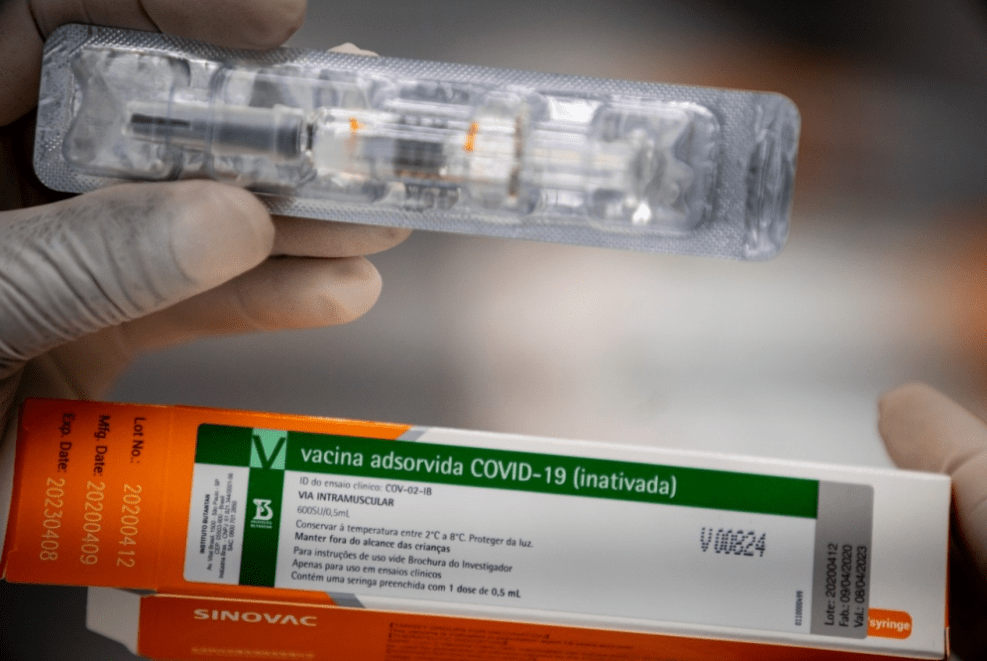
A Secretaria de Estado da Saúde Pública (Sesap) cominou, que devido à determinação da Agência Nacional de Vigilância Sanitária (Anvisa) neste sábado 4 sobre a interdição cautelar de lotes do imunizante Coronavac/Butantan, está orientando aos municípios potiguares que suspendam a aplicação da vacina.
O Rio Grande do Norte recebeu e distribuiu o lote número 202107101H, alvo da medida cautelar da Anvisa.
As unidades regionais de saúde do RN também estão sendo notificadas para suspender imediatamente qualquer eventual distribuição aos municípios.
A Sesap solicita que as unidades mantenham as vacina nas geladeiras à temperatura de +2 a +8, até o Ministério da Saúde emitir qualquer nova orientação.
Quanto aos municípios que já aplicaram as doses, devem aguardar também o posicionamento do MS para providências que se fizerem necessárias. Até o momento, segundo o RN+ Vacina, foram aplicadas 21 doses desse lote.
Por que a Anvisa resolveu proibir o uso dessas doses?
A informação veio direto do próprio Instituto Butantan no dia de ontem de que de fato alguns lotes, que em parte já tinham dado entrada no Brasil e outros que ainda vêm para o Brasil, tinham como local de fabricação uma fábrica não certificada pela Anvisa.
A príncipio, precisamos, pelo menos. que fosse comprovada a certificação por organismos regulatórios internacionais, que também seria uma informação útil para nós.
É muito importante deixar bem claro que não há processo investigativo ou de apuração, a informação veio do próprio Butantan. E diante dessa informação, não há outra coisa a fazer a não ser de maneira cautelar promover a interdição desses produtos que já estejam em território nacional até que essa certificação do fabricante seja devidamente apresentada e analisada.
Quais os próximos passos?
O que esperamos é que a certificação necessária seja enviada pela Sinovac ao Butantan, o Butantan deverá nos apresentar, analisaremos e emitiremos o parecer final. É importante a população saber que essa é uma decisão a nível de gerência e não a nível de diretoria.
Essa decisão é do escopo da Gerência Geral de Fiscalização. Do mesmo jeito que o registro de vacinas é também uma decisão gerencial da área de Medicamentos. Eu classificaria como um processo administrativo, regulatório, que pode acontecer.
E é uma medida cautelar para prevenir e evitar qualquer tipo de dúvida diante de um produto tão importante. Então não é nenhum demérito à vacina, nenhum senão em relação à marca. Nada disso.
A segurança da vacina pode ser colocada em suspeição?
A população pode ter tranquilidade em relação a esse episódio. Esse episódio mostra duas coisas muito claras: a informação veio do próprio Instituto Butantan, então ele foi transparente, colocou a informação para nós e, diante da informação, a agência, que tem a missão principal de proteger a saúde do cidadão, atuou imediatamente.
A palavra é tranquilidade. As instituições que têm que atuar nesse momento estão atuando. Estamos em diálogo com o Instituto Butantan e as respostas vão chegar.
Não há que se colocar nenhuma dúvida, descrédito, nada disso. As vacinas que são aprovadas no Brasil pela Anvisa seguiram avaliação rigorosa e tiveram como norte preceitos da OMS, que definiu as taxas de eficácia e parâmetros que precisam ser observados. A população não deve entender esse ato como nada além de cautela.
O RN já iria receber mais doses da coronavac
-

 Destaque7 dias ago
Destaque7 dias agoPrefeitura de São Rafael firma contrato milionário para gêneros alimentícios com empresa de fora e ignora comércio local
-

 Destaque1 dia ago
Destaque1 dia agoDenúncia aponta possível desvio de função no serviço público em São Rafael (RN)
-

 Geral6 dias ago
Geral6 dias agoPrefeitura de São Rafael abre inscrições para Campeonato Municipal de Futebol de Campo
